2
本剤は最低72時間空けて投与。 A法他の抗悪性腫瘍剤と併用で週2回,2週間 (1,4,8,11日目)投与後,10日間休薬 (12~21日目)。 これを1サイクルとし,2又は8サイクルまで繰り返す。 3又は9サイクル以降は週1回,2週間 (1,8日目)投与し,13日間休薬 (9~21日目)。 これを11/2 年2 月17 日 報道関係各位 東和薬品株式会社 11 成分23品目の製造販売承認を取得 東和薬品株式会社(本社:大阪府門真市、代表取締役社長:吉田逸郎)は、本日ジェネリック医薬品
ベルケイド インタビューフォーム
ベルケイド インタビューフォーム-ベルケイドの一般的に報告されている副作用のいくつかの例は次のとおりです。 吐き気や嘔吐などの消化器系の問題* 倦怠感(低エネルギー) 低レベルの赤血球、白血球、または血小板 皮膚の発疹 熱 *この副作用の詳細については、以下の「副作用の 規格単位 薬価 東和製品 ボルテゾミブ注射用3mg「トーワ」 東和薬品 3mg1瓶 先発・代表薬剤 ベルケイド注射用3mg

神ゲー攻略 第七章 掴んだ未来 Astlibra アストリブラ 生きた証 フリーゲーム フリーゲームと旅をする
ベルケイド注射用3mg VELCADE Injection ヤンセンファーマ D1024 円/瓶 毒薬, 処方箋医薬品 ※ 1 警告 11 本剤の投与は、緊急時に十分対応できる医療施設において、造血器悪性腫瘍又は全身性ALアミロイドーシスの治療に対して十分な知識・経験を1バイアル中 ボルテゾミブ 3mg 薬価 38,694円 / 1V 先発医薬品 ベルケイド注射用3mg 87,904円 / 1V 薬効分類名 抗悪性腫瘍剤(プロテアソーム阻害剤) 先発品との効能・効果、用法・用量の同異通常、成人に1日1回、ボルテゾミブとして13mg/m 2 (体表面積)を以下のA法又はB法で静脈内投与又は皮下投与する。 本剤は最低72時間空けて投与すること。 A法: 他の抗悪性腫瘍剤との併用において、週2回、2週間(1、4、8、11日目)投与した後、10日間
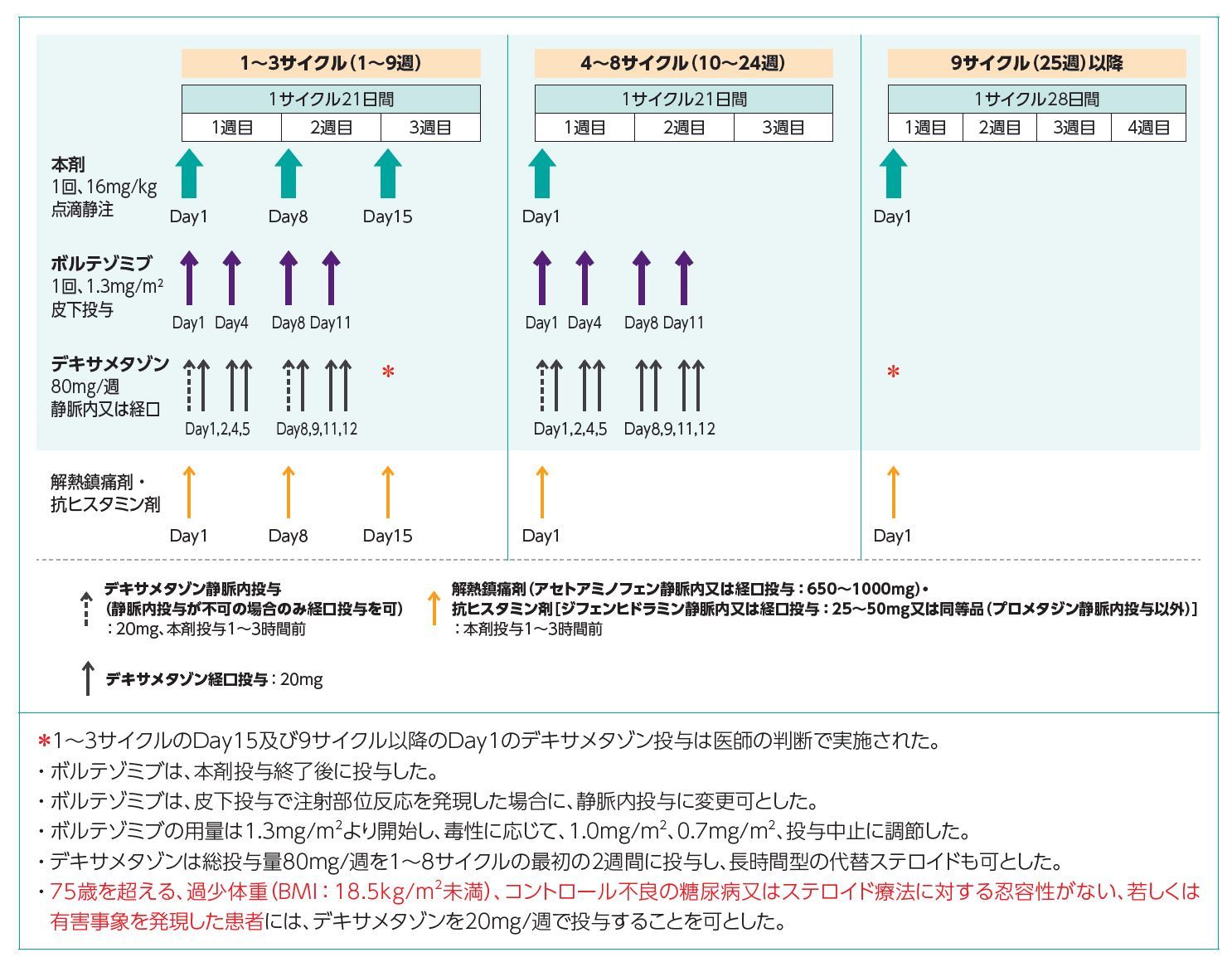
用法・用量 〈多発性骨髄腫〉 通常、成人に1日1回、ボルテゾミブとして13mg/㎡ (体表面積)を次のA法又はB法で静脈内投与又は皮下投与する。 本剤は最低72時間空けて投与すること。 A法: 他の抗悪性腫瘍剤との併用において、週2回、2週間 (1、4、8、11C ベルケイド®注射用3mgに関する注意事項 ベルケイド®注射用3mg(以下、本剤)適正使用及び患者さんの安全確保の観点から対象患者の選択、 適正使用基準及び治療期間中の注意事項を設定しました(P1:Decision tree)。 本剤の投与に際しては、治療上の必要性を十分に検討の上、本剤の投与の多発性骨髄腫:ベルケイド点滴day1,4,8,11/3wks 作用薬 数 日 か ら 数 週 間 数 週 間 以 降 ★★ 脱毛 ★ 食欲不振 ★★ 下痢 ★★ 時期 数日 点滴 のみ薬 今後の予定 主な副作用 注意点 レナデックスの内服後、発熱,頭痛,食欲不振, 脱力感,筋肉痛
ベルケイド インタビューフォームのギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 | Astlibra 生きた証 | Astlibra 生きた証 |
 Astlibra 生きた証 |  Astlibra 生きた証 | Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 |  Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 |  Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 |  Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 | Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 |  Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 | Astlibra 生きた証 | Astlibra 生きた証 |
Astlibra 生きた証 |  Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 | Astlibra 生きた証 |  Astlibra 生きた証 |
Astlibra 生きた証 |  Astlibra 生きた証 |  Astlibra 生きた証 |
 Astlibra 生きた証 |  Astlibra 生きた証 | Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 | Astlibra 生きた証 |
 Astlibra 生きた証 | Astlibra 生きた証 | Astlibra 生きた証 |
 Astlibra 生きた証 |  Astlibra 生きた証 |
ベルケイド®注射用3mgに関する注意事項 ベルケイド®注射用3mg(以下、本剤)適正使用及び患者さんの安全確保の観点から対象患者の選択、適 正使用基準及び治療期間中の注意事項を設定しました(P1:Decision tree)。 本剤の投与に際しては、治療上の必要性を十分に検討の上、本剤の投与の16 2 向井陽美, 他:臨床血液 11;
Incoming Term: ベルケイド インタビューフォーム,




0 件のコメント:
コメントを投稿